全球首個!我國新冠病毒中和抗體進入臨床試驗階段
央視網消息:由中國科學院微生物研究所等單位共同開發的重組全人源抗新冠病毒單克隆抗體注射液(以下簡稱“JS016”)近日獲國家藥監局批准,進入Ⅰ期臨床試驗。復旦大學附屬華山醫院完成了首例受試者給藥。這是全球首個在健康受試者中開展的新冠病毒中和抗體臨床試驗,候選新藥具有我國自主知識産權,旨在為探索JS016在人體中抗新冠病毒的治療與預防效果提供依據。
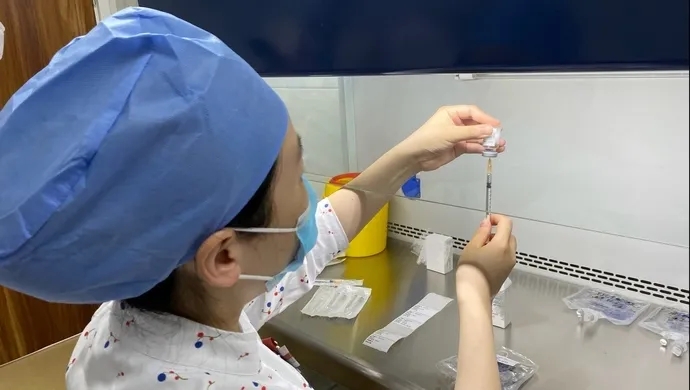
△華山醫院Ⅰ期臨床研究中心護士正在配製試本次試驗用藥品
這項臨床試驗採用隨機、雙盲、安慰劑對照研究方法,由華山醫院張菁教授與張文宏教授聯合主持,目的是評價JS016靜脈輸注給藥在中國健康志願者中的耐受性、安全性、藥代動力學特徵及免疫原性。
張文宏教授表示,中和抗體可針對新冠病毒精準進攻,具有獨特的靶向性,能阻止病毒在人體內複製,快速産生作用。希望在Ⅰ期臨床試驗中證明JS016良好的安全性和耐受性,為後續臨床計劃提供數據支持。中和抗體療法有望率先成為抗擊新冠病毒的治療選擇。
除了潛在的治療效果,中和抗體藥物還有望預防病毒感染。與疫苗不同,這種藥物更適用於應急狀態下重症監護病房的醫護人員、高齡老人等重點人群的預防。

△華山醫院本次臨床試驗項目的部分研究團隊成員
據介紹,這個候選新藥源自新冠肺炎康復期患者體內。中科院微生物研究所科研人員利用單細胞測序技術,從患者外周血單個核細胞中分離出新冠病毒中和性單克隆抗體;再利用流式細胞技術,進行阻斷試驗分析,篩選出中和活性很強的抗體並在體外重組表達。在科技部、上海市科委等部門支持下,君實生物對中科院微生物所篩選的抗體進行多路並行開發,完成了蛋白表達、免疫球蛋白Fc段(可結晶段)工程化改造、細胞株構建等抗體工藝開發和規模化生産的關鍵步驟。
在國務院聯防聯控機制統籌推進下,抗體研發工作得到了科技部、國家衛健委、國家藥監局、中科院、上海市、北京市的大力支持,上下聯動、協同攻關,體現出新型舉國體制在重大藥物研發方面的巨大優勢。
臨床前研究顯示,JS016對新冠病毒S蛋白的受體結合區域(RBD)表現出極高的特異性親和力,達到納摩爾水準,能夠搶先與病毒結合,從源頭上阻斷病毒入侵宿主細胞。
在有效性方面,恒河猴動物感染實驗表現出JS016的治療和預防效果,相關數據已在線發表于國際頂級科技雜誌《自然》。
在安全性方面,JS016抗體基因來源於康復病人單個B細胞,是全人源天然抗體,預計有較好的安全性。此外,為了減少抗體介導的急性肺損傷風險,確保臨床應用中的安全性,科研團隊對JS016進行Fc段改造,有效降低了可能存在的抗體依賴增強效應(ADE)、抗體介導的細胞毒作用以及細胞吞噬效應。臨床前食蟹猴毒理學研究中,最大耐受劑量、未觀察到明顯毒性反應劑量是人體臨床試驗推薦起始劑量的數十倍,意味著存在較大的安全窗。(總臺央視記者 竇筠韻)


